Завдяки особливим фізичним і хімічним властивостям каолін є незамінним неметалевим мінеральним ресурсом у виробництві кераміки, паперу, гуми, пластмас, вогнетривів, нафтопереробки та інших галузях промисловості, сільського господарства та національної оборони. Білизна каоліну є важливим показником його застосовної цінності.

Фактори, що впливають на білизну каоліну
Каолін - це різновид дрібнозернистої глини або глиняної породи, яка в основному складається з мінералів каолініту. Його кристалохімічна формула 2SiO2 · Al2O3 · 2H2O. Невелику кількість неглинистих мінералів становлять кварц, польовий шпат, мінерали заліза, титану, гідроксид і оксиди алюмінію, органічні речовини тощо.
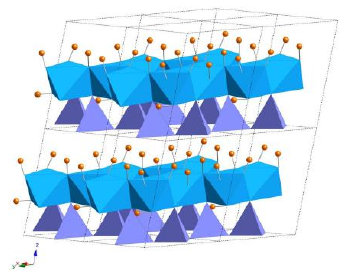
Кристалічна структура каоліну
За станом і природою домішок у каоліні домішки, що викликають зменшення білизни каоліну, можна розділити на три категорії: органічний вуглець; Пігментні елементи, такі як Fe, Ti, V, Cr, Cu, Mn тощо; Темні мінерали, такі як біотит, хлорит та ін. Як правило, вміст V, Cr, Cu, Mn та інших елементів у каоліні невеликий, що мало впливає на білизну. Мінеральний склад і вміст заліза і титану є основними факторами, що впливають на білизну каоліну. Їх існування вплине не тільки на природну білизну каоліну, а й на його кальциновану білизну. Зокрема, наявність оксиду заліза негативно впливає на колір глини, знижує її яскравість і вогнестійкість. І навіть якщо кількість оксиду, гідроксиду і гідратованого оксиду оксиду заліза становить 0,4%, цього достатньо, щоб надати глинистому осаду червоне-жовте забарвлення. Такими оксидами та гідроксидами заліза можуть бути гематит (червоний), маггеміт (червоно-коричневий), гетит (коричнево-жовтий), лімоніт (помаранчевий), гідратований оксид заліза (коричнево-червоний) тощо. Можна сказати, що видалення домішок заліза в каоліні відіграє надзвичайно важливу роль у кращому використанні каоліну.
Стан виникнення елемента заліза
Ступінь вмісту заліза в каоліні є основним фактором, що визначає спосіб видалення заліза. Велика кількість досліджень припускає, що кристалічне залізо у формі дрібних частинок змішується з каоліном, тоді як аморфне залізо покривається поверхнею дрібних частинок каоліну. В даний час стан заліза в каоліні поділяється на два типи вдома та за кордоном: один - у каолініті та допоміжних мінералах (таких як слюда, діоксид титану та іліт), який називається конструкційним залізом; Інший у формі незалежних мінералів заліза, які називають вільним залізом (включаючи поверхневе залізо, дрібнозернисте кристалічне залізо та аморфне залізо).

Залізо, видалене шляхом видалення заліза та відбілювання каоліну, є вільним залізом, головним чином включаючи магнетит, гематит, лімоніт, сидерит, пірит, ільменіт, ярозит та інші мінерали; Більшість заліза існує у формі високодисперсного колоїдного лимоніту, а невелика кількість у формі сферичного, голчастого та неправильного гетиту та гематиту.
Метод знезалізнення та відбілювання каоліном
Розділення води
Цей метод в основному використовується для видалення уламкових мінералів, таких як кварц, польовий шпат і слюда, і більш грубих домішок, таких як уламки гірських порід, а також деяких мінералів заліза і титану. Мінерали-домішки з подібною щільністю та розчинністю до каоліну неможливо видалити, а покращення білизни є відносно неочевидним, що підходить для збагачення та відбілювання відносно високоякісної каолінової руди.
Магнітна сепарація
Мінеральні домішки заліза в каоліні зазвичай слабомагнітні. В даний час в основному використовується метод високоградієнтної сильної магнітної сепарації, або слабкі магнітні мінерали перетворюються на сильний магнітний оксид заліза після випалу, а потім видаляються звичайним методом магнітної сепарації.

Вертикальний кільцевий високоградієнтний магнітний сепаратор

Високоградієнтний магнітний сепаратор для електромагнітного шламу

Низькотемпературний надпровідний магнітний сепаратор
Метод флотації
Метод флотації застосований для очищення каоліну первинних і вторинних родовищ. У процесі флотації частинки каолініту та слюди відокремлюються, а очищені продукти є декількома придатними промисловими сировинними матеріалами. Селективне флотаційне розділення каолініту та польового шпату зазвичай проводять у суспензії з контрольованим pH.
Метод скорочення
Метод відновлення полягає у використанні відновника для відновлення домішок заліза (таких як гематит і лімоніт) у тривалентному стані каоліну до розчинних іонів двовалентного заліза, які видаляються шляхом фільтрації та промивання. Видалення домішок Fe3+ з промислового каоліну зазвичай досягається шляхом поєднання фізичної технології (магнітної сепарації, селективної флокуляції) та хімічної обробки в кислих або відновних умовах.
Гідросульфіт натрію (Na2S2O4), також відомий як гідросульфіт натрію, ефективний у відновленні та вилуговуванні заліза з каоліну, і в даний час використовується в каоліновій промисловості. Однак цей метод необхідно проводити в сильних кислотних умовах (pH<3), що призводить до високих експлуатаційних витрат і впливу на навколишнє середовище. Крім того, хімічні властивості гідросульфіту натрію нестабільні, що вимагає спеціальних і дорогих умов зберігання та транспортування.
Діоксид тіосечовини: (NH2) 2CSO2, TD) є сильним відновником, який має такі переваги, як сильна відновна здатність, екологічність, низька швидкість розкладання, безпека та низька вартість серійного виробництва. Нерозчинний Fe3+ в каоліні можна відновити до розчинного Fe2+ через TD.
Згодом білизну каоліну можна збільшити після фільтрації та промивання. TD дуже стабільний при кімнатній температурі та нейтральних умовах. Сильну відновну здатність TD можна отримати лише за умов сильної лужності (pH>10) або нагрівання (T>70 °C), що призводить до високої вартості експлуатації та труднощів.
Метод окислення
Окислювальна обробка включає використання озону, перекису водню, перманганату калію та гіпохлориту натрію для видалення шару адсорбованого вуглецю для покращення білизни. Каолін у глибшому місці під більшою товщиною розкриву має сірий колір, а залізо в каоліні знаходиться у відновному стані. Використовуйте сильні окислювачі, такі як озон або гіпохлорит натрію, щоб окислити нерозчинний FeS2 у піриті до розчинного Fe2+, а потім промийте, щоб видалити Fe2+ із системи.
Метод кислотного вилуговування
Метод кислотного вилуговування полягає в перетворенні нерозчинних домішок заліза в каоліні в розчинні речовини в кислих розчинах (соляної кислоти, сірчаної кислоти, щавлевої кислоти та ін.), таким чином реалізуючи виділення з каоліну. Порівняно з іншими органічними кислотами щавлева кислота вважається найбільш перспективною через її кислотну силу, хорошу комплексоутворювальну властивість і високу відновну здатність. За допомогою щавлевої кислоти розчинене залізо може бути осаджено з розчину для вилуговування у формі оксалату двовалентного заліза та може бути додатково оброблено з утворенням чистого гематиту шляхом прожарювання. Щавлеву кислоту можна дешево отримати з інших промислових процесів, а на стадії випалу керамічного виробництва будь-який залишковий оксалат в обробленому матеріалі розкладатиметься на вуглекислий газ. Багато дослідників вивчали результати розчинення оксиду заліза щавлевою кислотою.
Метод високотемпературного прожарювання
Кальцинація - це процес виробництва каоліну спеціального сорту. Відповідно до температури обробки виробляють два різних сорти кальцинованого каоліну. Прожарювання в діапазоні температур 650-700 ℃ видаляє структурну гідроксильну групу, а водяна пара, що виділяється, підвищує еластичність і непрозорість каоліну, що є ідеальним атрибутом для нанесення покриття на папір. Крім того, шляхом нагрівання каоліну при 1000-1050 ℃ можна не тільки збільшити стираемість, але й отримати 92-95% білизни.
Прожарювання хлоруванням
Залізо і титан були видалені з глинистих мінералів, особливо каоліну, шляхом хлорування, і були отримані хороші результати. У процесі хлорування та прожарювання при високій температурі (700 ℃ - 1000 ℃) каолініт піддається дегідроксилюванню з утворенням метакаолініту, а при вищій температурі утворюються фази шпінелі та муліту. Ці перетворення підвищують гідрофобність, твердість і розмір частинок шляхом спікання. Мінерали, оброблені таким чином, можна використовувати в багатьох галузях промисловості, таких як виробництво паперу, ПВХ, гуми, пластмас, клеїв, полірування та зубної пасти. Вища гідрофобність робить ці мінерали більш сумісними з органічними системами.
Мікробіологічний метод
Технологія мікробного очищення мінералів є відносно новим предметом переробки корисних копалин, включаючи технологію мікробного вилуговування та технологію мікробної флотації. Технологія мікробного вилуговування мінералів – це технологія екстракції, яка використовує глибоку взаємодію між мікроорганізмами та мінералами для руйнування кристалічної решітки мінералів і розчинення корисних компонентів. Окислений пірит та інші сульфідні руди, що містяться в каоліні, можуть бути очищені за допомогою технології мікробної екстракції. Зазвичай використовувані мікроорганізми включають Thiobacillus ferrooxidans і Fe-відновлюючі бактерії. Мікробіологічний метод має низьку вартість і низьке забруднення навколишнього середовища, що не вплине на фізико-хімічні властивості каоліну. Це новий метод очищення та відбілювання з перспективою розвитку мінералів каоліну.
Резюме
Видалення заліза та відбілювання каоліну потребує вибору найкращого методу відповідно до різних причин забарвлення та різних цілей застосування, покращення повної білизни мінералів каоліну та надання йому високої споживчої та економічної цінності. Майбутня тенденція розвитку повинна полягати в органічному поєднанні характеристик хімічного методу, фізичного методу та мікробіологічного методу, щоб повністю відобразити їхні переваги та стримати недоліки та недоліки, щоб досягти кращого ефекту відбілювання. У той же час також необхідно продовжити вивчення нового механізму різних методів видалення домішок і вдосконалити процес, щоб видалення заліза та відбілювання каоліну розвивалися в напрямку екологічного, ефективного та низьковуглецевого.
Час публікації: 02.03.2023

